0.5 mLになったピュアバックス® の安全性と有効性
今までと変わらぬ優れた安全性と有効性で、より扱いやすくなりました
1. 既存の1 mL製剤との比較
1 mLと比較して局所反応は有意に少ないことが示されました
【前臨床試験】
■ 目的
既存の1 mL製剤と0.5 mL製剤の局所反応の大きさを比較する
■ 供試動物
8〜11週齢のSPF猫20頭
□ 1 mL群:10頭
□ 0.5 mL群:10頭
■ 方法
□ 0日目(D0)と28日目(D28)に1 mLまたは0.5 mLを接種
□ 各回15分後に局所反応(腫脹)の大きさを観察
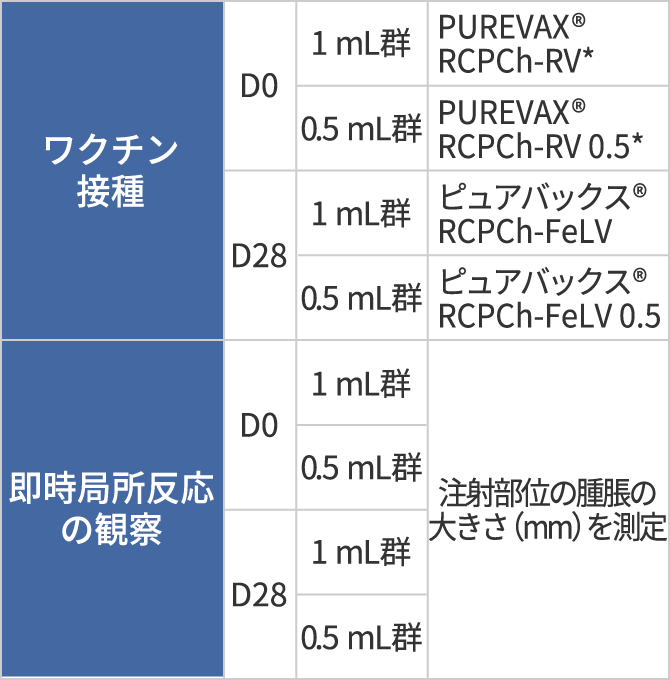
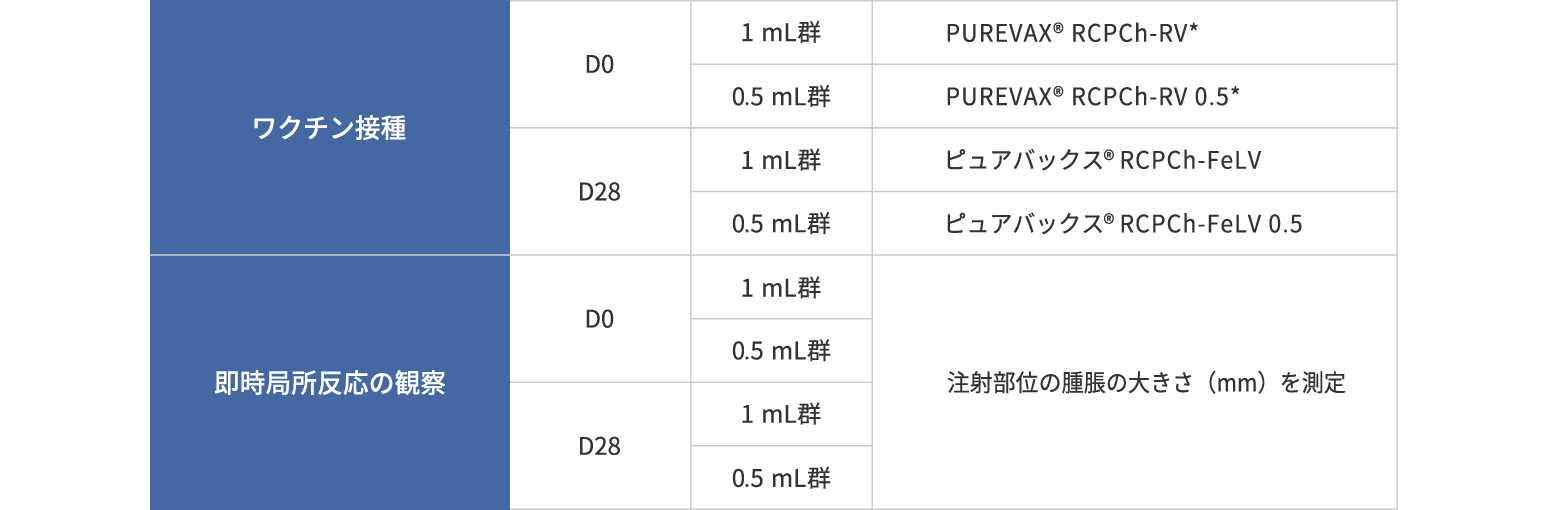
■ 結果
□ D0においての 0.5 mL群の方が有意に小さかった(p<0.05)
□ D28において1 mL群では2/10頭に腫脹を認めたが、0.5 mL群では認めなかった
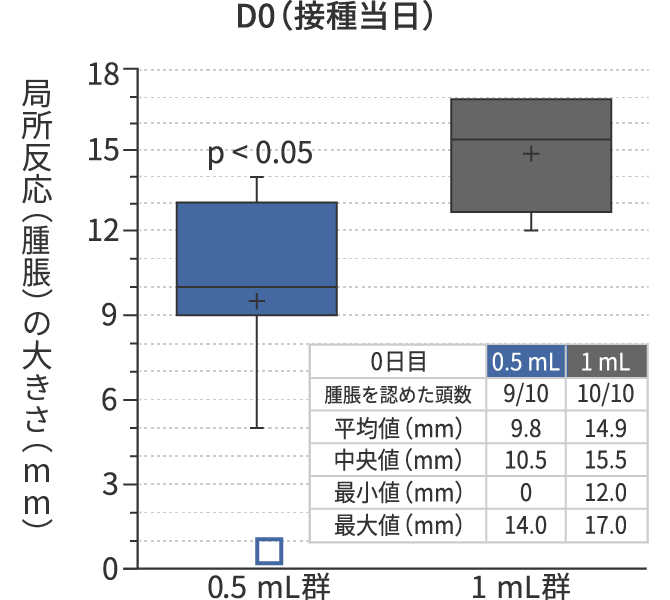
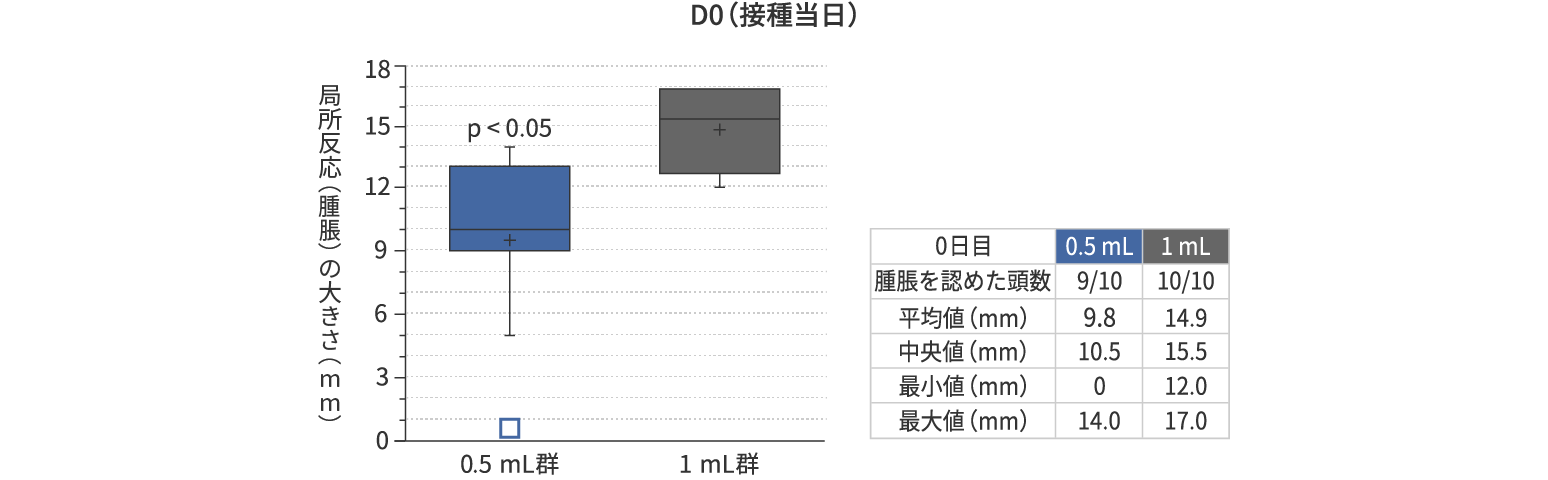
Jas D. et al. Vaccine. 2021 Feb 12:39(7):1051-1057.
既存の1 mL製剤と比較して局所反応は有意に少ないことが示された
*日本国内で承認されているピュアバックス® RCPCh-FeLVの液状ワクチンの主剤を狂犬病ウイルス由来防御抗原蛋白発現遺伝子導入カナリア痘ウイルス(vCP65株)に置き換えたもので、主剤以外は ピュアバックス® RCPCh-FeLVと同一である。日本では未承認製剤(EUでは承認済み)で、液状ワクチンの容量が0.5 mLと1 mLの2種類がある。RCPChの成分に対して狂犬病ウイルス成分の影響がないことを確認している
2. 既存のピュアバックス® RCPCh-FeLV(1 mL)との比較
1 mLと0.5 mLで副反応の発生率は同等であり、変わらぬ安全性が示されました
【フランスの野外臨床試験】
■ 目的
既存の1 mL製剤と0.5 mL製剤の局所反応の発生率を比較する
■ 供試動物
フランスの複数の動物病院に来院した8週齢以上の猫398頭
□ 1 mL*群 :初年度接種62頭 + 追加接種39頭(計101頭)
□ 0.5 mL**群:初年度接種186頭 + 追加接種111頭(計297頭)(1 mL:0.5 mLの頭数は約1:3)
* 既存のピュアバックス® RCPCh-FeLV(1 mL)
** 新しいピュアバックス® RCPCh-FeLV 0.5(0.5 mL)
■ 方法
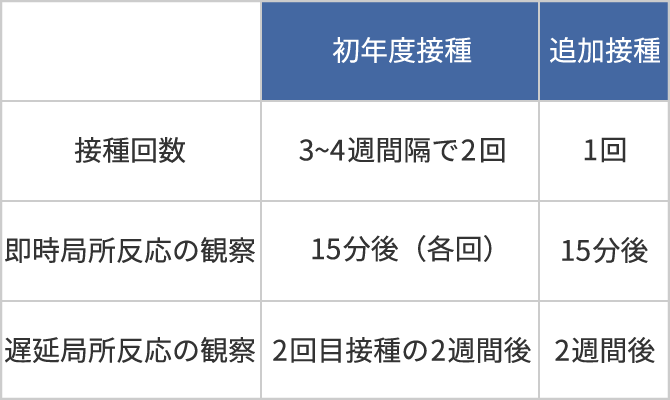
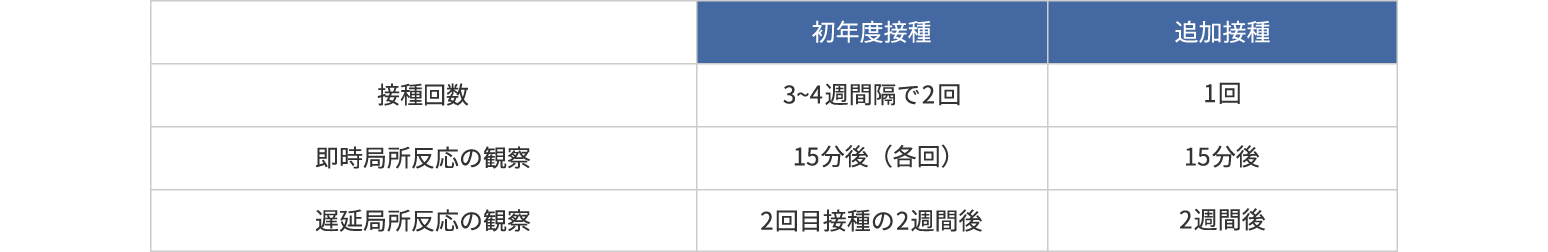
■ 結果
既存の1 mL製剤と同等の安全性を示した
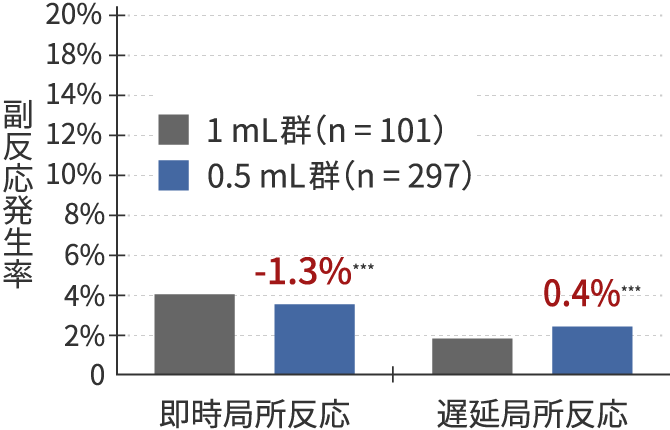
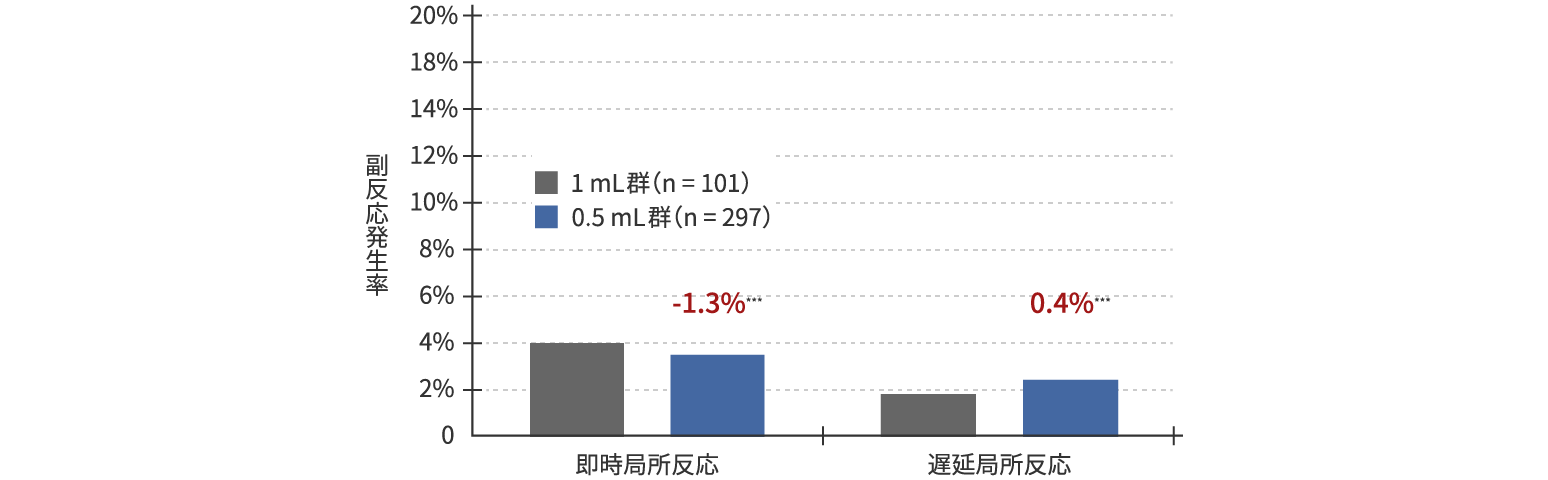
*** リスク差 0.0%(0.5 mL群の副反応発生率と1 mL群の副反応発生率の差)
Jas D, et al. Vaccine. 2021 Feb 12:39(7):1051-1057.
3. アジュバント加4種混合ワクチン*(1 mL)とピュアバックス® RCP-FeLV 0.5(0.5 mL)との比較
アジュバント加ワクチンと比較して局所反応は有意に少ないことが示されました
【局所反応の比較試験】
■ 目的
アジュバント加4種混合ワクチン(1 mL)とピュアバックス® RCP-FeLV 0.5(0.5 mL)の局所反応を比較する
■ 供試動物
10〜32ヵ月齢のSPF猫30頭
□ アジュバント加4種混合ワクチン(1 mL)群:15頭
□ ピュアバックス® RCP-FeLV 0.5(0.5 mL)群:15頭
■ 方法
右後肢大腿部皮下に1 mLまたは0.5 mLのワクチンを、左後肢大腿部皮下に1 mL または0.5 mLの生理食塩水を接種した。接種日を0日目(D0)として3週間毎日観察し、1週間ごとの注射部位スコア**の合計を求めた。また、 7日目(D7)と21日目(D21)に 皮膚生検を実施した(結果は示さず)
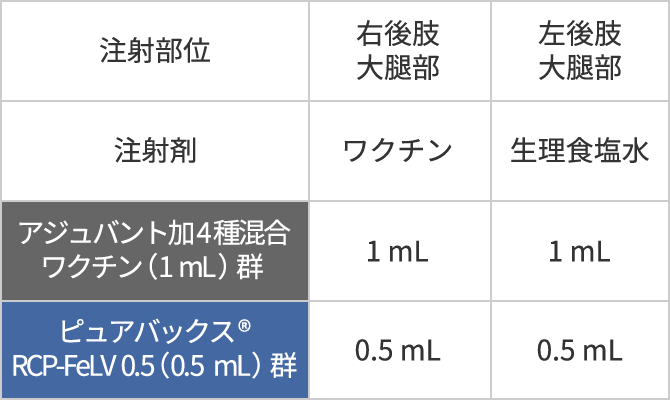
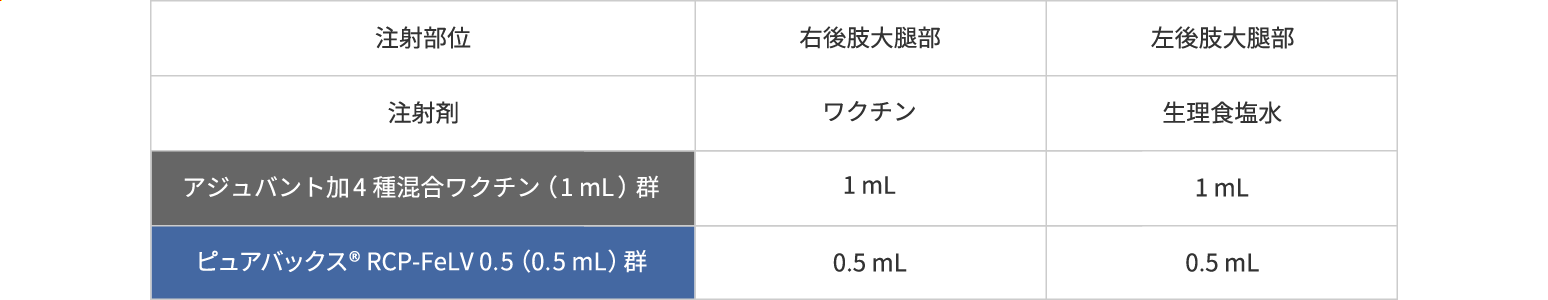
* 3種混合生ワクチンをアジュバント加FeLVコンポーネントワクチンで溶解して接種する。 日本では未承認製剤
** 注射部位の腫脹、発赤、疼痛、 掻痒についてそれぞれ4段階でスコア化したもの
■ 結果
ピュアバックス® RCP-FeLV 0.5の方が局所反応の頻度、程度、持続時間がそれぞれ有意に低かった
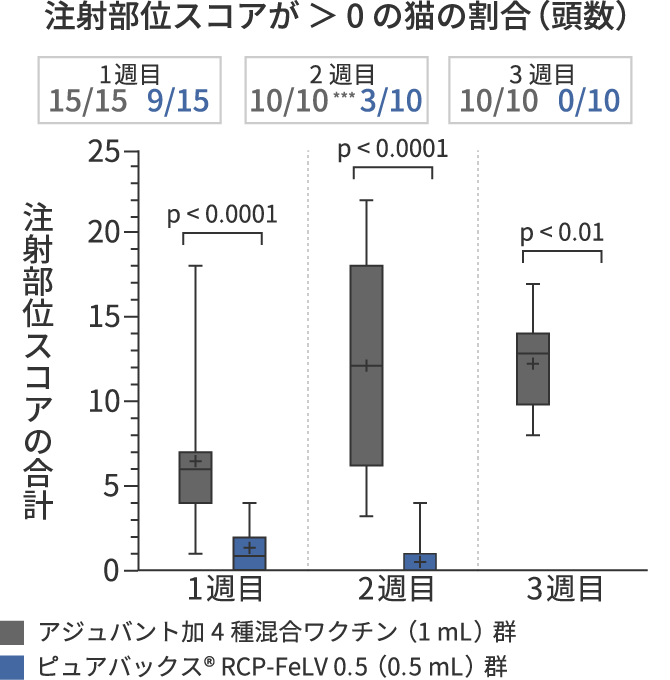
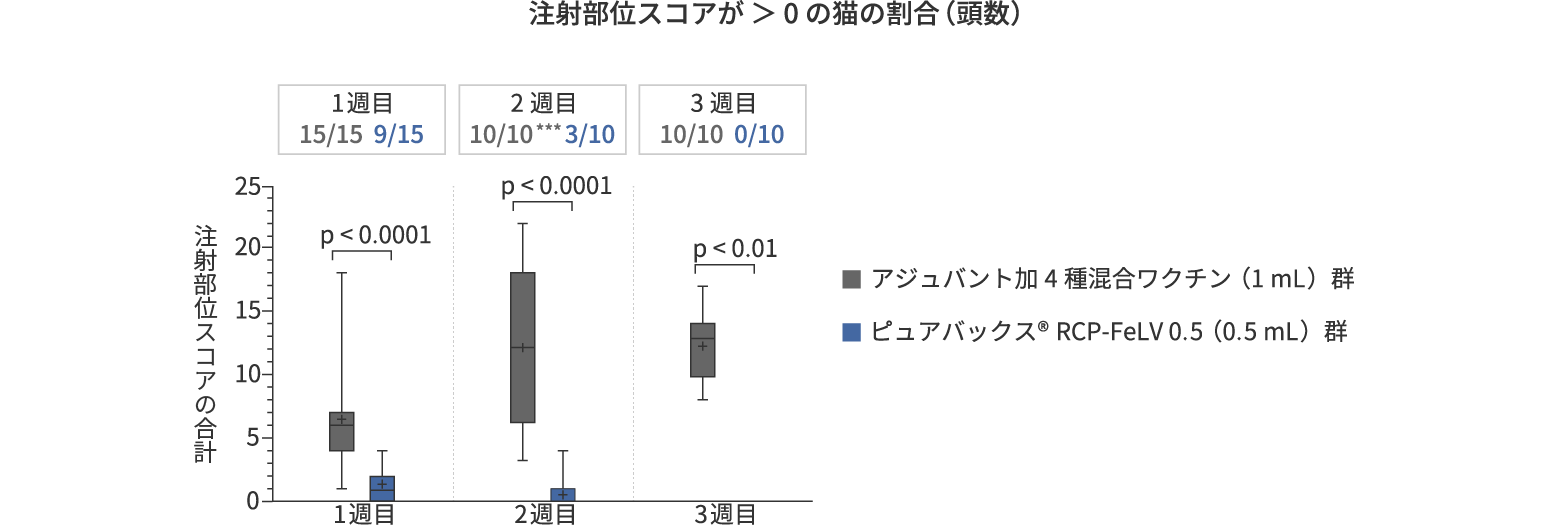
*** D7で皮膚生検に供した各群5頭は以後の観察から除外した
Haist V, et al. Vaccine. 2023 Jul 19:41(32):4752-4761.
4. ノンアジュバント(安全性へのこだわり)
ピュアバックス® RCPCh-FeLVはアジュバント加ワクチンと比較して有意に炎症スコアが低下していた。
接種後の好中球+マクロファージ+リンパ球の浸潤スコアの合計
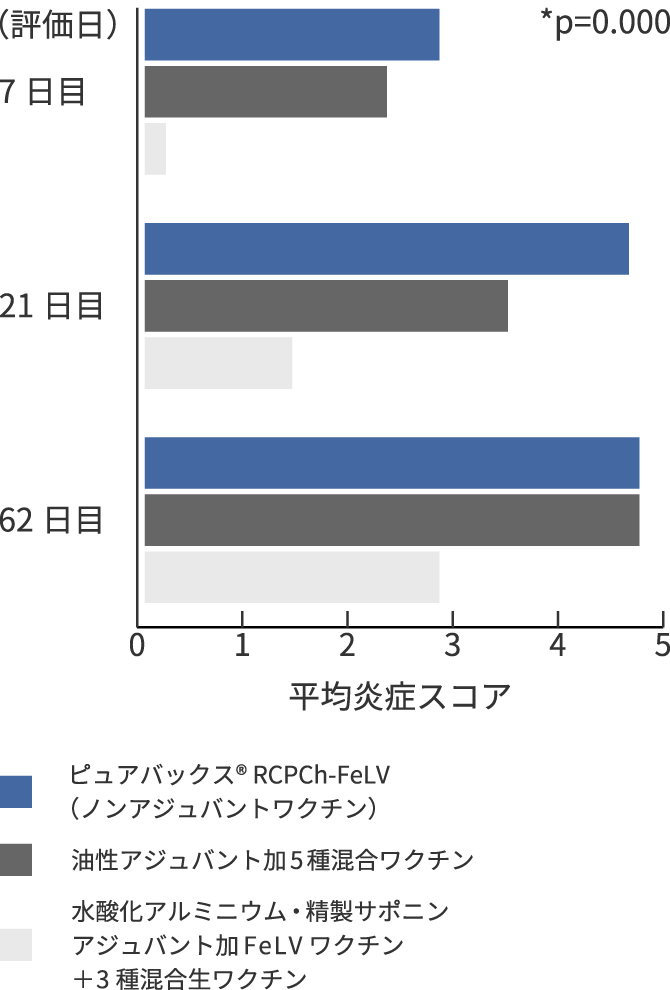

Day MJ, et al, Vaccine, 2007 May 16:25(20):4073-84.を基にグラフを作成
5. 病原性復帰の可能性があるカリシウイルスは、不活化で2株使用し幅広い抗原域を実現
ピュアバックス®に含まれるFCVワクチンは、G1株と431株の組合せによる相乗効果により、日本分離株やVS-FCV*を含む野外株の93%(55株/59株)を中和した。
*virulent systemic FCV:強毒全身性猫カリシウイルス
FCVワクチン株の抗血清を用いたFCV野外株 **に対する交差中和試験
** 強毒全身性猫カリシウイルス(VS-FCV)株を含む複数の地域から分離されたFCV野外株を使用
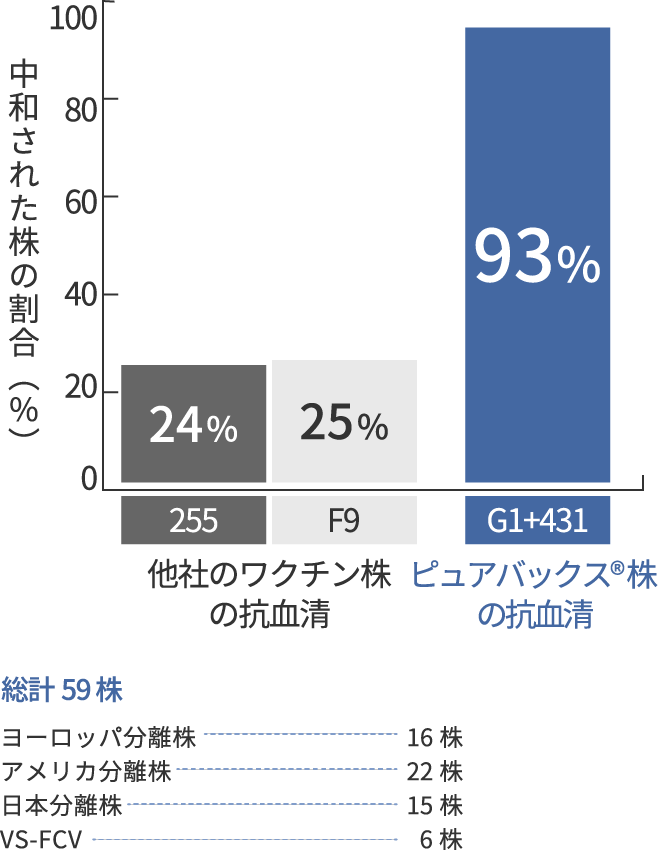
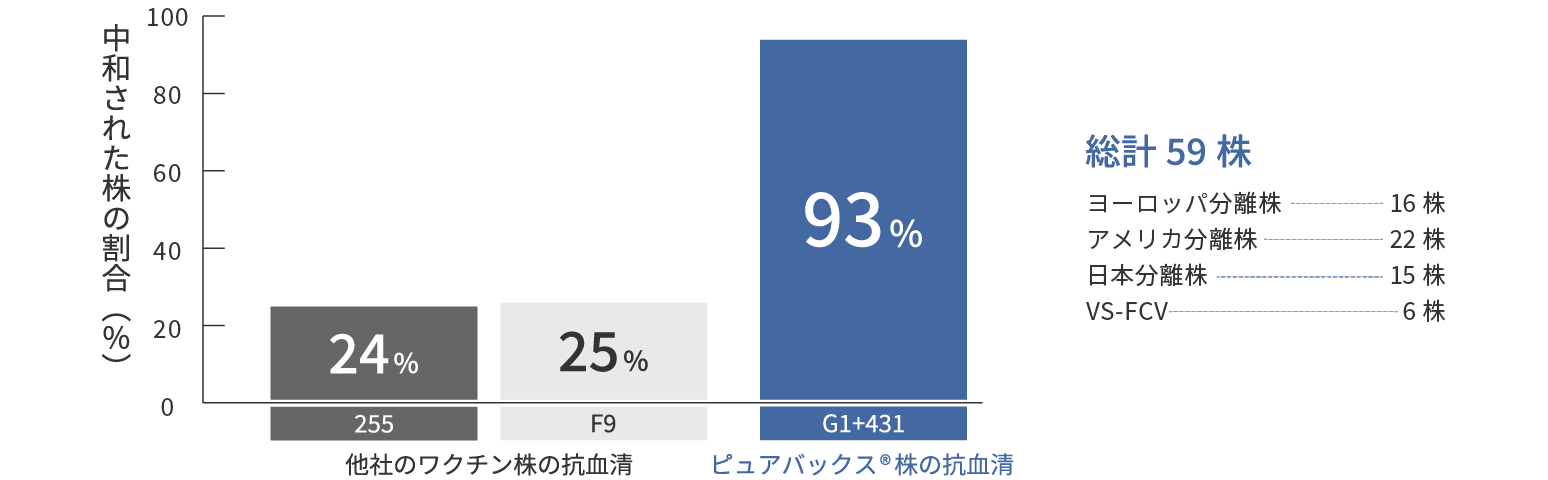
Poulet H, et al. Vaccine. 2008 Jul 4:26(29-30):3647-54. を基にグラフを作成
6. FeLVに対する高い防御効果
カナリア痘ウイルスベクターを使用する理由
- 「細胞性免疫」と「液性免疫」の両方を誘導する
- アジュバントが不要

©ベーリンガーインゲルハイムアニマルヘルス
先進的なカナリア痘ウイルスベクターワクチンテクノロジー
ピュアバックス®のFeLVワクチンにはFeLV由来防御抗原蛋白を発現する遺伝子を導入したカナリア痘ウイルス(vCP97株)がベクターとして用いられている
カナリア痘ウイルスベクターワクチンの機序
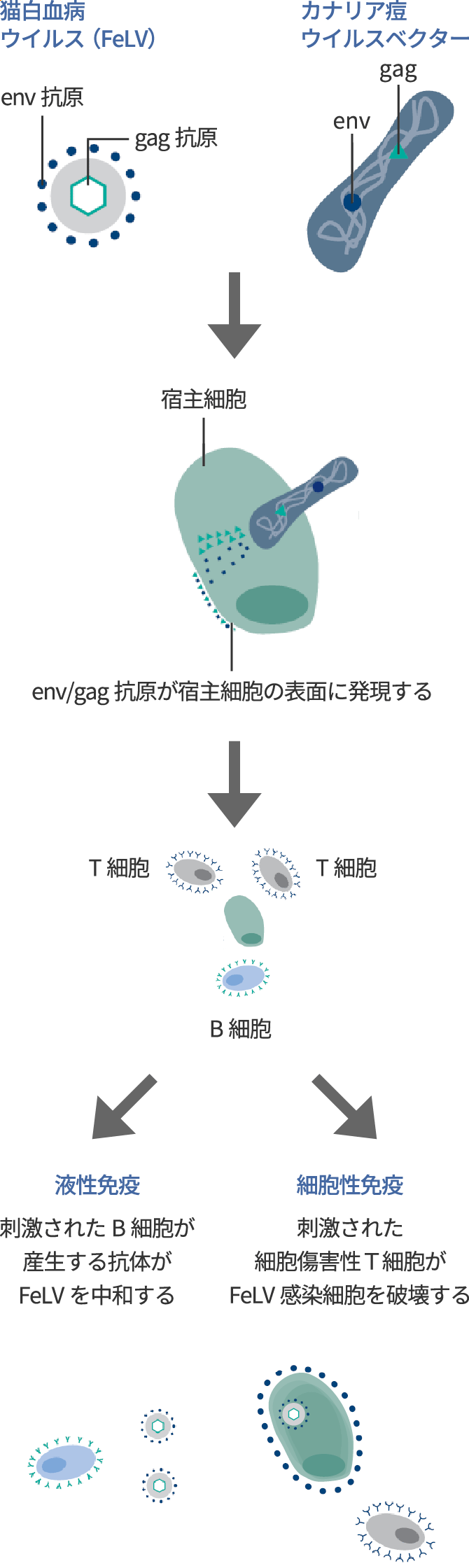

カナリア痘ウイルスベクターが宿主細胞と融合後、標的抗原が宿主細胞の表面に発現する
ノンアジュバントでありながら細胞性免疫と液性免疫の両方を強力に誘導する
先進のベクターワクチンテクノロジー
ベクターワクチンの作用機序